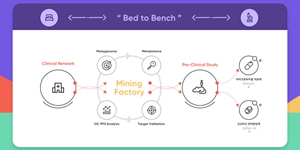
▲ '지노클(GENOCLE)' 신규 표적 발굴 플랫폼 원리 설명도. <지노앤컴퍼니>
지놈앤컴퍼니는 면역항암제 후보물질 ‘GENA-104’가 식품의약품안전처로부터 임상 1상 시험 계획(IND) 승인을 받았다고 10일 밝혔다.
GENA-104는 신규 표적 발굴 플랫폼 ‘지노클(GENOCLE)’을 통해 발굴한 신규 타깃 ‘CNTN4’을 표적으로 삼는 물질이다.
CNTN4가 면역 T세포 활성을 억제하는 것을 차단해 효과적으로 암세포를 사멸한다.
지놈앤컴퍼니는 전임상 과정에서 일부 환자들이 겪는 기존 면역항암제 비반응 현상의 원인이 CNTN4에 있다는 것을 확인했다.
이를 해결할 수 있는 신규타깃 항암제의 가능성을 확인하고 2021년부터 2023년까지 3년 연속으로 미국 암연구학회(AACR)에 연구결과를 발표했다.
이번 임상 1상은 고형암 환자를 대상으로 진행된다. ‘단계적 용량 증량 코호트(dose escalation)’를 통해 안전성과 내약성을 입증하고 유효성을 확인한다.
배지수 지놈앤컴퍼니 대표이사는 “지놈앤컴퍼니는 CNTN4라는 신규 타깃을 최초로 발굴했다”며 “이를 타깃으로 하는 CENA-104는 기존 면역항암제에 효과를 보지 못하는 환자의 미충족 의료 수요를 해결하는 치료제가 될 수 있을 것”이라고 말했다.
GENA-104는 지난해 12월 국가신약개발사업단의 10대 우수과제로 선정된 바 있다. 손영호 기자








![[현장] 일본판 쥬라기공원 '정글리아' 가보니, 어른도 혹할 '공룡 세계'는 진행형](https://businesspost.co.kr/news/photo/202605/20260511154758_246164.png)


