![한미약품, 근손실 최소화한 차세대 비만 치료제 미국서 임상 1상 들어가]()
| ▲ 한미약품이 3일 미국 FDA로부터 차세대 비만치료제와 관련해 임상1상 IND를 받았다. 차세대 비만치료 삼중작용제 관련 이미지. <한미약품> |
[비즈니스포스트] 한미약품이 차세대 비만치료 삼중작용제 임상 1상을 본격화한다.
한미약품은 3일(현지시각) 미국 식품의약국(FDA)에서 차세대 비만 치료 삼중작용제(LA-GLP/GIP/GCG) ‘HM15275’(코드명)의 임상 1상 진입을 위한 임상시험계획(IND)을 승인 받았다고 7일 밝혔다.
이번 임상 시험에서는 건강한 성인 및 비만 환자를 대상으로 HM15275의 안전성과 내약성, 약동학, 약력학 특성 등을 평가한다.
한미약품은 “오랜 기간 대사성 질환 분야에서 쌓아온 R&D 역량을 토대로 속도감 있게 임상 개발을 추진할 것”이라며 “HM15275를 최단 기간 내 상용화하는 것이 목표”라고 설명했다.
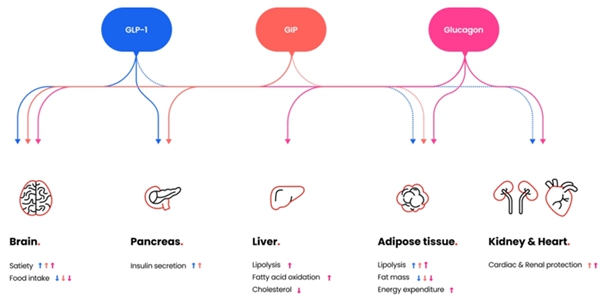
HM15275는 차세대 비만 신약이다. 글루카곤 유사 펩타이드(GLP-1)와 위 억제 펩타이드(GIP), 글루카곤(GCG) 등 각각의 수용체 작용을 최적화해 비만 치료에 특화돼 있는 물질로 평가받는다.
GLP-1 수용체 작용제는 포만감을 증가시켜 체중을 감소시키고 인슐린 분비와 감수성을 개선해 혈당 조절을 원활하게 한다. GIP는 GLP-1 수용체 작용제의 약리학적 이점을 향상시키면서 메스꺼움과 구토, 설사 등 이 작용제의 일반적인 위장관 부작용을 완화할 수 있다. 글루카곤은 포만감 조절과 함께 에너지 소비 및 지질 대사 조절에도 관여한다.
한미약품은 “이 세 가지 약리작용을 적절히 활용하면 비만뿐 아니라 제2형 당뇨병 및 심혈관 질환에 대한 치료 잠재력을 극대화할 수 있다”고 덧붙였다.
한미약품은 해당 약물과 관련해 6월 미국에서 열리는 2024 미국당뇨병학회(ADA)에서 HM15275에 대한 4건의 비임상 연구 결과를 발표할 예정이다.
최인영 한미약품 R&D센터장은 “HM15275에는 한미가 인크레틴 분야에서 20년 이상 연구를 지속하면서 축적한 연구 지식과 노하우들이 집약돼 있다”며 “전 세계적 사회 문제로 대두되고 있는 ‘비만’ 영역에서 치료 효과를 혁신적으로 높인 차세대 신약 개발을 완수할 수 있도록 연구에 더욱 매진하겠다”고 말했다. 장은파 기자